
[KIMIA XII SEMESTER 1] SIFAT KOLIGATIF LARUTAN ELEKTROLIT YouTube
Jumlah partikel larutan elektrolit lebih banyak daripada larutan non-elektrolit sehingga sifat koligatifnya pun akan lebih besar. Nilai dari sifat koligatif larutan non-elektrolit dapat diketahui dengan rumus-rumus berikut ini: Penurunan tekanan uap. ΔP = P⁰.

Contoh Soal Perbandingan Penurunan Titik Beku (Sifat Koligatif Larutan Elektrolit) YouTube
Soal nomor 4. Berapakah derajat ionisasi larutan elektrolit lemah biner dengan konsentrasi 0,1 M pada suhu 27 o C dan tekanan osmotik 4,305. π = M . R . T { 1 + (n-1) α} Jadi larutan biner tersebut mempunyai derajat ionisasi sebesar 0,75. Demikian ulasan mengenai sifat koligatif larutan slektrolit, soal, dan pembahasannya. Semoga manfaat.

Rangkuman Materi Sifat Koligatif Larutan Kimiazainal
Jadi, itulah rumus sifat koligatif larutan elektrolit dalam gaya penulisan jurnalistik santai. Dengan memahami konsep ini, kita dapat menikmati manfaatnya dalam kehidupan sehari-hari, baik dalam minuman sejuk di hari yang panas atau secangkir kopi yang nikmat di pagi hari.

Rangkuman Materi Sifat Koligatif Larutan
Pengertian Sifat Koligatif Larutan. Sifat koligatif larutan adalah sifat fisik larutan yang hanya bergantung pada jumlah partikel zat terlarut. Sebelum mempelajari lebih lanjut, kita harus mengetahui jenis-jenis konsentrasi larutan terlebih dahulu, karena dalam perhitungannya akan banyak melibatkan rumus-rumus konsentrasi.

5. Sifat Koligatif Larutan Elektrolit
Di konsenterasi yang sama, sifat koligatif larutan elektrolit memiliki jumlah nilai yang lebih besar dibandingkan sifat koligatif larutan non elektrolit, dan banyaknya partikel-partikel zat terlarut hasil dari reaksi ionisasi larutan elektrolit ini bisa dirumuskan didalam faktor Van't Hoff, untuk perhitungan sifat koligatif larutan elektrolit.

Apakah Air Kapur Termasuk Larutan Elektrolit / Larutan elektrolit kuat adalah larutan yang
1. Satuan Konsentrasi Larutan. Pembelajaran pertama yang harus kamu pahami adalah satuan konsentrasi larutan. Dalam materi ini, kamu akan mempelajari hal-hal yang digunakan untuk menganalisis sifat koligatif larutan yaitu molalitas, molaritas, & fraksi mol. Jika didefinisikan, molalitas adalah banyaknya mol zat pelarut yang ada dalam 1 kg.

Larutan Elektrolit dan Non Elektronik Beserta Contoh Elektrolit Belajar IPA
Sifat koligatif larutan merupakan sifat larutan yang bergantung pada banyaknya zat terlarut dan tidak tergantung pada jenis zat terlarut. Sifat koligatif larutan dibagi menjadi dua jenis, yaitu: sifat koligatif larutan elektrolit dan larutan non elektrolit. Sifat Koligatif Larutan Elektrolit 1. Kenaikan titik didih ∆Tb = Kb . m { 1 + (n-1) α} Keterangan: ∆Tb =

8 Rumus Sifat Koligatif Larutan Elektrolit dan Non Elektrolit Materi Kimia
Pada larutan non-elektrolit faktor van't Hoff nya bernilai 1 karena tidak memiliki ion, sehingga tidak diperlukan faktor van't Hoff dalam perhitungan sifat koligatifnya. Sifat koligatif pada larutan elektrolit sama dengan sifat koligatif non-elektrolit yaitu penurunan tekanan uap jenuh, kenaikan titik didih, penurunan titik beku, dan.

Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10
Perbedaan mendasar dengan rumus penurunan tekanan uap pada larutan non elektrolit adalah adanya faktor Van't Hoff yang disimbolkan dengan huruf "i".. Sifat koligatif larutan elektrolit seperti penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik dipengaruhi oleh faktor Van't Hoff (i)..

Rumus Sifat Koligatif Larutan Dan Contoh Soal Contoh Makalah
Jenis Sifat Koligatif Larutan. Sifat kologatif larutan terdiri dari empat jenis yakni: penurunan tekanan uap jenuh, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik. Berikut penjelasannya dirangkum dari laman resmi Jurusan Manajemen Pertanian Lahan Kering (MPLK) Polteknik Petanian Negeri Kupang (Politanikoe) dan Buku Kimia Fisika.

sifat koligatif larutan elektrolit teori YouTube
A. Pengertian Sifat Koligatif Larutan. Sifat koligatif larutan adalah sifat yang bergantung pada konsentrasi molekul atau ion zat terlarut, tetapi tidak bergantung pada jenis zat terlarutnya. Sifat koligatif meliputi empat hal yaitu: Penurunan Tekanan Uap. Penurunan Titik Beku. Kenaikan Titik Didih.

Contoh Soal Sifat Koligatif Larutan Elektrolit Dan Non Elektrolit Riset
Dalam menghitung nilai sifat koligatif larutan elektrolit kita dapat menggunakan persamaan-persamaan dalam larutan nonelektrolit dengan menambahkan faktor Van't Hoff. Nilai faktor Van't Hoff merupakan perbandingan antara efek koligatif larutan elektrolit dengan efek koligatif larutan nonelektrolit pada konsentrasi yang sama. Selain itu, faktor Van't Hoff juga dapat ditentukan dengan.

Sifat Koligatif Larutan Penurunan Titik Beku Sains Kimia Unamed
Sel Elektrolisis: Contoh Soal Reaksi Redoks dan Rumus Hukum Faraday | Kimia Kelas 12. Contoh Sel Volta: Leclanche, Baterai Perak Oksida, Merkurium, dan Proses Korosi | Kimia Kelas 12. Berikut ini rumus sifat koligatif larutan elektrolit, non-elektrolit, diagram P-T, molalitas, fraksi mol, tekanan uap jenuh, titik beku, titik didih, osmotik.
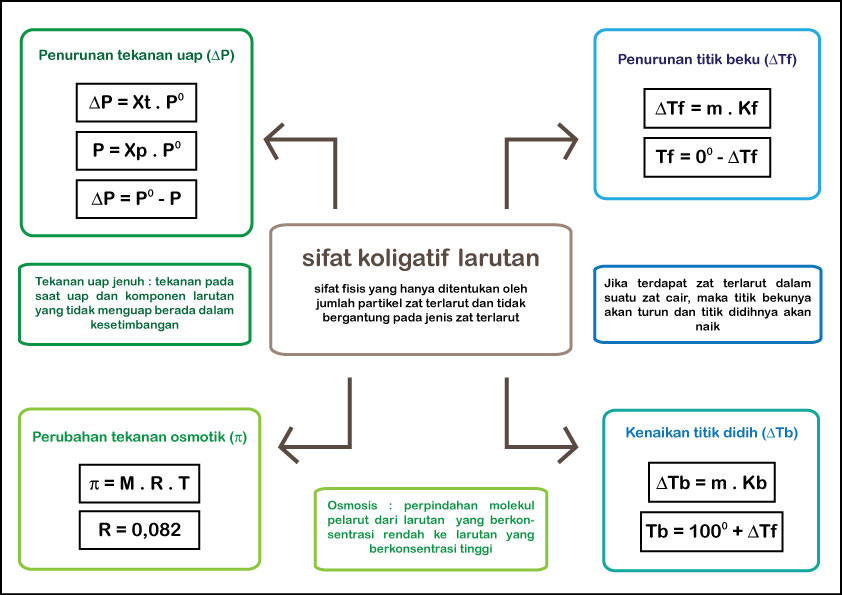
The Chemsquad Headquarters Weapon 1 Sifat Koligatif Larutan
Sifat koligatif sendiri hanya memandang "kuantitas", bukan "kualitas". Oleh sebab itu, sifat larutan, seperti rasa, warna, dan kekentalan (viskositas) merupakan sifat-sifat yang bergantung pada jenis zat terlarut yang tercampur dalam larutan. Terdapat empat sifat koligatif larutan, yaitu penurunan tekanan upa, kenaikan titik didih.

PPT SIFAT KOLIGATIF LARUTAN PowerPoint Presentation, free download ID4367326
Sifat koligatif larutan terdiri dari dua jenis, yaitu sifat koligatif larutan elektrolit dan sifat koligatif larutan nonelektrolit Sifat koligatif larutan juga dikelompokan menjadi 4, yaitu: 1. Penurunan tekanan uap jenuh (Δ Tp) 2. Kenaikan titik didih (ΔTb) 3.. Larutah non elektrolit: Larutan elektrolit: Rumus umum: Δ p = Pº - P:

Rumus Sifat Koligatif Larutan Elektrolit Dan Non Elektrolit PDF
Meskipun sifat koligatif melibatkan larutan, sifat koligatif tidak bergantung pada interaksi antara molekul pelarut dan zat terlarut, tetapi bergatung pada jumlah zat terlarut yang larut pada suatu larutan. Sifat koligatif terdiri dari penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik. 1. Penurunan Tekanan Uap.